Uutta tietoa sähkökemiallisista reaktioista11.12.2023 9.42
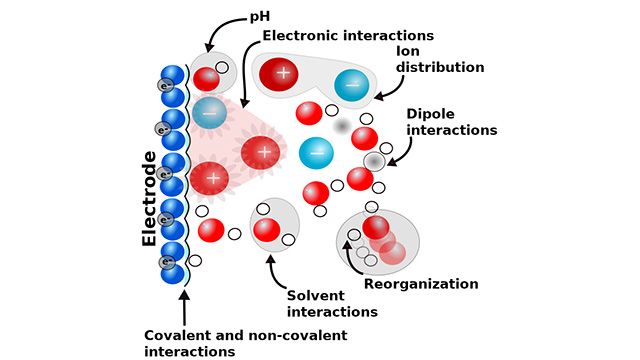
Sähkökemialliset reaktiot ovat keskeisiä vihreässä siirtymässä. Nämä reaktiot hyödyntävät sähkövirtaa ja sähköistä potentiaalieroa kemiallisten reaktioiden aikaansaamiseksi, mahdollistaen sähköisen energian sitomisen ja vapauttamisen kemiallisista sidosten avulla. Tämä luo perustan monille kemiallisille sovelluksille, kuten vetyteknologialle, akuille sekä erilaisille ratkaisuille kemiallisen kiertotalouden saralla. Näiden sovellusten kehittäminen edellyttää syvällistä ymmärrystä sähkökemiallisista reaktioista sekä niihin vaikuttavista tekijöistä. Viimeaikaiset tutkimukset ovat osoittaneet, että käytetty liuotin, sen happamuus sekä käytetyt elektrolyytti-ionit vaikuttavat keskeisesti elektrodin ohella sähkökemiallisten reaktioiden tehokkuuteen. Tutkimus keskittyykin nykyisin alla olevassa kuvassa kuvattujen sähkökemiallisten rajapintojen eli elektrodin ja elektrolyytin muodostaman reaktioympäristön ymmärtämiseen. Hiilidioksidin muutamista hiilineutraaliksiRajapintojen ymmärtäminen pelkästään kokeellisin menetelmin on kuitenkin äärimmäisen haastavaa, sillä rajapinnat ovat hyvin ohuita, alle nanometrin paksuisia. Laskennalliset ja teoreettiset menetelmät ovat nykyisin keskeisiä, sillä ne tarjoavat tehokkaan tavan tutkia sähkökemiallisten rajapintojen ominaisuuksia atomitasolla ja ajan suhteen. Jyväskylän yliopiston kemian laitoksella on tehty pitkäjänteistä menetelmäkehitys- ja laskentatyötä, joiden ansiosta ymmärretään syvällisemmin sähköisten rajapintojen kemiaa, erityisesti elektrolyytti-ionien vaikutusta. - Kaksi tuoreinta tutkimusartikkeliamme keskittyvät elektrolyyttien vaikutukseen hapen ja hiilidioksidin pelkistysreaktioissa, jotka ovat keskeisiä polttokennojen toiminnalle, vetyperoksidin valmistamiselle sekä hiilidioksidin muuntamiseksi hiilineutraaleiksi kemikaaleiksi ja polttoaineiksi, kertoo akatemiatutkija Marko Melander Jyväskylän yliopiston kemian laitokselta. Tutkimus yhdisti kokeelliset ja laskennalliset tuloksetJyväskylän yliopiston kemian laitoksen tutkijat ovat tehneet yhteistyötä kansainvälisten kokeellisten ja laskennallisten ryhmien kanssa, mikä on mahdollistanut elektrolyyttivuorovaikutusten yksityiskohtaisen tutkimisen. Viimeaikaisia tutkimustuloksia on julkaistu alan arvostetuissa lehdissä Nature Communications ja Angewandte Chemie International Edition. - Molemmissa julkaisuissa olemme keskittyneet perustutkimukseen, joka vaatii äärimmäisen tarkkoja ja vaativia mittaustekniikoita ja niiden yhdistämistä uusinta osaamista vaativiin simulaatioihin. Pystyimme esimerkiksi ensimmäistä kertaa yhdistämään vedyn kvanttimekaaniseen luonteeseen perustuvien kineettisten isotooppiefektien mittaamisen ja simuloinnin, mikä auttoi yhdistämään kokeelliset ja laskennalliset tulokset. Käytimme myös uusia menetelmiä ionien ja liuottimen uudelleenjärjestäytymisen simuloimiseksi, mikä syvensi ymmärrystämme näiden yhteisvaikutuksesta reaktiomekanismiin, kertoo Melander. Uutta tietoa sähkökemiallisesta reaktiostaTutkimuksen avulla opittiin ymmärtämään useita mekanismeja, joilla elektrolyytit vaikuttavat sähkökemiallisiin reaktioihin. Yksi näistä tavoista on ionien sitoutuminen reagoivaan molekyylin, kuten kuvassa 2 on esitetty. - Osoitimme erityisesti, että ionit säätelevät sekä elektrodipinnan että rajapinnan läheisyydessä olevan liuottimen rakennetta ja dynamiikkaa ei-sitovien vuorovaikutusten avulla. Nämä vuorovaikutukset määrittävät reaktiopolun, nopeuden ja valikoituvuuden eli sen, mitä sähkökemiallisessa reaktiossa muodostuu ja kuinka tehokkaasti, kertoo Melander.  Mahdollisuuksia kehittää uusiutuvia energiateknologioitaVaikka tutkimus keskittyi elektrolyyttien sekä sähköisten rajapintojen perustutkimukseen, voi se edistää parempien sähkökemiallisten teknologioiden kehittämistä. - Erityisesti ioni- ja liuotinvuorovaikusten hyödyntäminen voi auttaa säätämään sähkökemiallisten reaktioiden nopeutta ja valikoituvuutta. Elektrolyytin muuttaminen voi ohjata esimerkiksi hapen pelkistysreaktiota joko polttokennoihin tai vetyperoksidin valmistamiseen sopivaksi. Elekrolyyttikemia voi auttaa myös hiilidioksidin pelkistystä tuottamaan haluttuja, arvokkaampia tuotteita, kertoo Melander. Artkkelien tiedot:
|